Annale eg2 CAP Petite Enfance 2014
Ci-dessous vous trouverez l'épreuve générale Mathématiques et Sciences physiques de l'année 2014. Si vous cherchez tous les annales eg2 du CAP PE pour vous entraînez, vous pouvez les télécharger ainsi que leurs corrigés sur notre page dédiée. C'est gratuit.
CAP Mathématiques-Sciences
Session 2014
Durée : 2h00
Coefficient : 2
SUJET
Mathématiques : 10 points
La Terre est surnommée la planète bleue, car elle est la seule planète du système solaire à posséder autant d’eau. On distingue : l’eau salée qui forme les mers ainsi que les océans, et l’eau douce qui forme notamment les rivières et les lacs.
Exercice 1 : (3 points)
1.1. Sachant que 97,2 % de l’eau sur Terre est salée, calculez le pourcentage que représente l’eau douce.
…
1.2. Complétez le tableau ci-dessous donnant la répartition de l’eau douce disponible suivant son origine.
Origine |
Fréquence (en %) |
Angle en degré (arrondir à l’unité) |
|
Rivières |
5,6 |
20° |
|
Eau atmosphérique |
6,4 |
…… |
|
Eau dans le sol |
21,9 |
…… |
|
Lacs |
…… |
…… |
|
TOTAL : |
100 |
360° |
1.3. Complétez le diagramme à secteurs circulaires correspondant à la répartition de l’eau douce disponible suivant son origine.
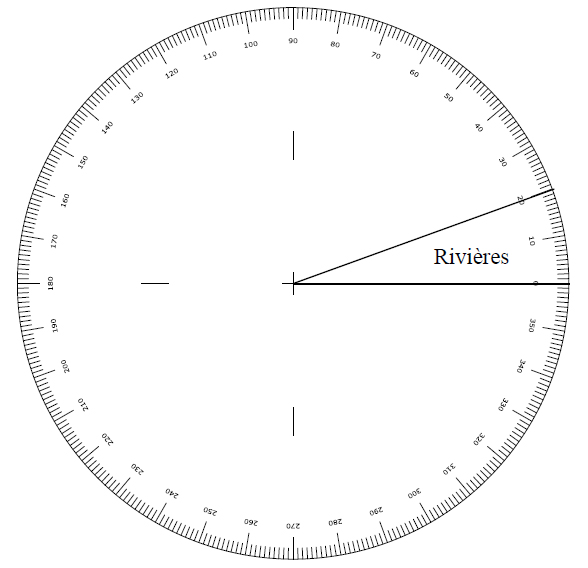
Exercice 2 : (4,5 points)
Plusieurs techniques permettent d’obtenir de l’eau douce à partir de l’eau salée. On souhaite étudier le coût de deux d’entre elles : l’osmose et la distillation afin de choisir la plus rentable.
Le coût de production d’un m3 d’eau traitée par osmose est 0,40 €.
2.1. On note V le volume d’eau traitée en m3, et P le coût de production correspondant en €.
Complétez le tableau ci-dessous pour la technique par osmose.
|
Volume d’eau V (en m3) |
50 |
100 |
200 |
…… |
400 |
500 |
|
Prix P (en €) |
…… |
40 |
…… |
120 |
…… |
200 |
2.2. Placez les points de coordonnées (V ; P) du tableau précédent dans le repère ci-dessous.
Tracez la droite D1 passant par ces points correspondant à la technique par osmose.
La droite D2 déjà tracée représente le coût de production de la technique par distillation.
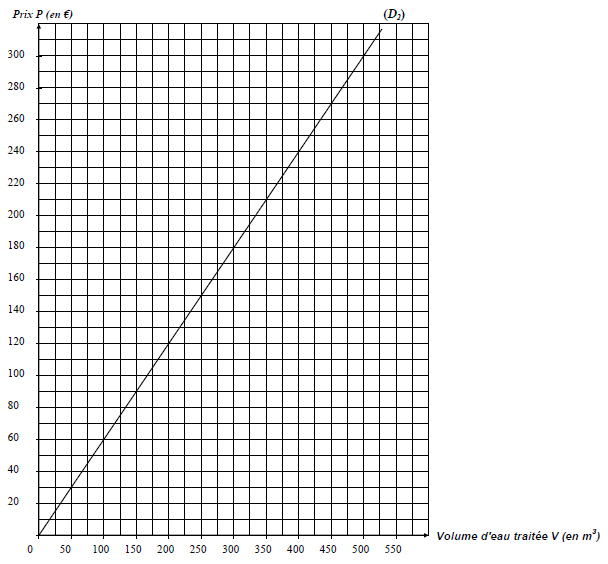
2.3. Utilisation de la représentation graphique ci-dessus.
2.3.1. Déterminez, en laissant apparents les traits utiles à la lecture, le prix à payer, en €, pour traiter par la technique de distillation 500 m3 d’eau.
…
2.3.2. Déterminez, à l’aide du graphique précédent, la technique de traitement la moins coûteuse. Justifiez la réponse.
…
2.4. M. Mario est maire d’une commune de 2 000 habitants dont les ressources en eau douce sont très faibles. Il s’interroge sur le coût de la production d’eau douce par la technique de l’osmose.
Il estime la consommation moyenne en eau par habitant et par jour à 250 L.
2.4.1. Quel est le volume d’eau nécessaire, en m3, pour subvenir, chaque jour, aux besoins des habitants de cette commune ? On rappelle que 1 m3 = 1 000 L.
...
...
2.4.2. Quel sera, en €, le coût de cette production d’eau ? (1 m3 d’eau traitée par osmose coûte 0,40 €)
....
Exercice 3 : (2,5 points)
Afin de stocker l’eau traitée après dessalement, M. Mario doit étudier la mise en place d’un réservoir dont la capacité minimale est de 1 000 m3. Il consulte un modèle dont le schéma est donné ci- dessous :
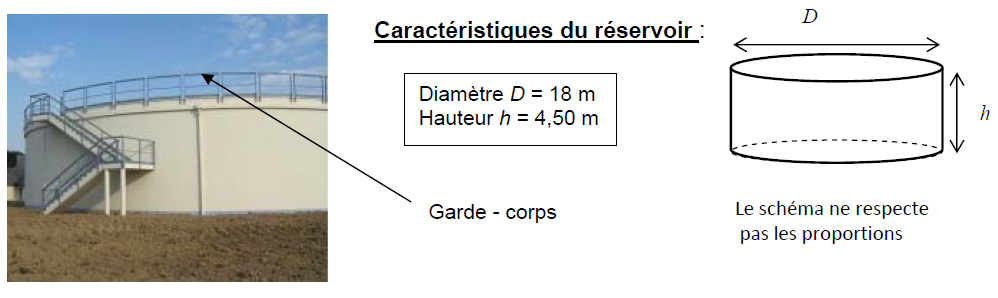
3.1. Cochez le nom du solide correspondant à la forme du réservoir.
cube cylindre prisme
3.2. Calculez, en m², l’aire A1 de la base de ce solide. On donne A1 = π x R2
Arrondir le résultat au centième.
....
3.3. En prenant : A1 = 254 m2 , calculez, en m3, le volume V de ce réservoir.
On donne : V = A1 x h
...
3.4. Indiquez si le modèle de réservoir choisi par M. Mario convient. Justifiez votre réponse.
...
3.5. Afin de protéger les agents d’entretien d’une chute, M. Mario décide de faire installer un garde- corps en haut du réservoir.
Calculez la longueur de ce garde-corps. On donne : l = 2 x π x R . Arrondir le résultat à l’unité.
...
Sciences Physiques : 10 points
Exercice 4 : (6 points)
On souhaite savoir si une eau après un dessalement contient encore des ions chlorure. Pour cela, on réalise un test de reconnaissance de l’ion chlorure sur cette eau.
Voici le tableau de quelques tests d’identification d’ions :
Nom de l’ion |
Formule de l’ion |
Test utilisé pour le reconnaître |
||
|
Réactif mis en contact avec l’ion |
Observation |
|||
ion cuivre |
Cu2+ |
soude |
formation d’un précipité bleu |
|
ion fer II |
Fe2+ |
soude |
formation d’un précipité verdâtre |
|
|
ion aluminium |
Al3+ |
soude |
formation d’un précipité blanc |
|
ion chlorure |
Cl- |
nitrate d’argent |
formation d’un précipité blanc (qui noircit à la lumière) |
|
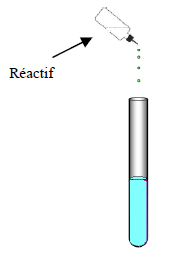
4.1. Donnez le nom du réactif permettant de mettre en évidence l’ion chlorure.
................................................................................................................................................................................................
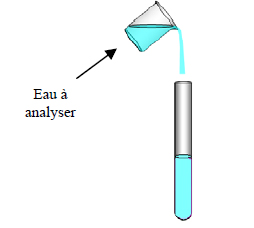
4.2. Décrivez les étapes de l’expérience permettant de reconnaître l’ion chlorure.
Nommez les éléments de verrerie utilisés.
 |
………………………………………………………………………………… ………………………………………………………………………………… ………………………………………………………………………………… ………………………………………………………………………………… ………………………………………………………………………………… |
 |
………………………………………………………………………………… ………………………………………………………………………………… ………………………………………………………………………………… ………………………………………………………………………………… ………………………………………………………………………………… |
4.3. On observe la formation d’un précipité blanc qui noircit à la lumière.
Indiquez si l’eau testée contient des ions chlorure. Justifiez votre réponse.
....
4.4. Complétez le tableau suivant indiquant le nom ainsi que le nombre des éléments chimiques présents dans le nitrate d’argent de formule AgNO3.
|
Symbole de l’élément chimique |
Ag |
N |
O |
|
Nom de l’élément chimique |
Argent |
Azote |
|
|
Nombre d’éléments |
1 |
4.5. Calculez, en g/mol, la masse molaire moléculaire du nitrate d’argent AgNO3.
On donne : M(Ag) = 108 g/mol ; M(N) = 14 g/mol ; M(O) = 16 g/mol.
...
4.6. Le nitrate d’argent est corrosif. Sur son flacon figure le pictogramme suivant :
Indiquez une des précautions à respecter lors de l’utilisation de ce produit.
...
4.7. Pour l’eau potable, la concentration maximale en ions chlorure fixée par une directive est 250 mg/L. Convertissez cette concentration en g/L.
....
4.8. Grâce à un dosage, on a trouvé qu’il y avait 0,15 g/L d’ions chlorure dans l’eau analysée.
L’eau analysée est-elle conforme aux exigences de la directive précédente ? Justifiez votre réponse.
....
Exercice 5 : (4 points)
Dans un village d’Afrique du Nord, le Centre de Développement des Énergies Renouvelables a installé une unité de dessalement d’eau fonctionnant à l’énergie solaire.
L’apport d’énergie est assuré par un générateur photovoltaïque qui est composé de panneaux solaires. On souhaite vérifier que le générateur photovoltaïque fournira suffisamment d’énergie pour alimenter l’installation.
Chaque panneau solaire a une puissance maximale de 38 W.
5.1. Calculez, en W, la puissance maximale du générateur photovoltaïque sachant qu’il comprend 72 panneaux solaires.
...
5.2. Le générateur fonctionne 5 heures à sa puissance maximale.
Déterminez, en Wh, l’énergie produite E1. On rappelle la relation E = P × t avec E en Wh, P en W et t en heure.
...
Les différents éléments de l’installation consomment une puissance électrique totale de 1 700 W.
5.3. Vérifiez que l’énergie nécessaire E2 pour alimenter l’installation pendant 8 heures est 13 600 Wh.
...
L’unité de stockage et de régulation accumule l’énergie tout au long du temps de fonctionnement du générateur à l’aide de batteries.
5.4. Le fonctionnement durant 5 heures du générateur photovoltaïque suffit-il à fournir suffisamment d’énergie pour alimenter l’installation de dessalement pendant 8 heures.
Justifiez votre réponse.
...
La tension d’alimentation de l’installation est continue ; elle est comprise entre 110 V et 134 V.
5.5. Donnez le nom d’un appareil permettant de mesurer une tension électrique.

....
5.6. Choisissez entre : 200 mV, 2 V, 20 V, 200 V et 600 V le calibre le plus adapté pour mesurer la tension d’alimentation de l’installation.
....
5.7. Justifiez votre choix fait à la question précédente.
...
5.8. Entourez les bornes de connexion utilisées sur l’appareil de mesure pour relever la tension.
|
VΩ |
COM |
mA |
10 A |
Besoin d'aide pour préparer votre CAP Petite enfance ?
Pour les personnes souhaitant être accompagnées, il existe la préparation à distance au CAP PETITE ENFANCE AEPE et au CONCOURS ATSEM. Par ailleurs, l'organisme à distance vous aidera dans vos démarches de recherche de structure d'accueil pour vos stages.
CAP PETITE ENFANCE AEPE
- Accessible partout : Oui (France et DROM-COM)
- Alternance : Possible
- Durée : 500 heures
- Stage : 14 semaines
- Conditions d'accès : Dès 16 ans
- Adapté aux adultes : Oui
- Adapté aux reconversions professionnelles : Oui
- Suivi et accompagnement par des professeurs : Oui
- Début session : quand vous le voulez
- Tarif : 57,60 € / mois
- Financements acceptés : CPF / Pôle Emploi
- 100% e-learning
Prépa Concours ATSEM
- Accessible partout : Oui (France et DROM-COM)
- Durée : 500 heures
- Prérequis : être titulaire du CAP Petite Enfance ou avoir une dérogation
- Conditions d'accès : Dès 16 ans
- Adapté aux adultes : Oui
- Adapté aux reconversions professionnelles : Oui
- Suivi et accompagnement par des professeurs : Oui
- Début session : quand vous le voulez
- Tarif : 43,30€ / mois
- 100% e-learning
